DRUID HILLS – Die Tatsache, daß nach der Verabreichung vom mRNA-Wirkstoffen nun erstmals Herzmuskelentzündungen im vorpubertären Alter wird von der US-Gesundheitsbehörde CDC dadurch kleinrelativiert, daß diese Fälle im Vergleich zur Menge der verabreichten Dosen selten seien. Daraufhin zieht Pfizer eine Zulassung des Wirkstoffs für Unter-5-Jährige zurück.
US-Gesundheitsbehörde stapelt tief
Der ersten offiziellen Untersuchung zu den Folgen der Impfung von 5-12-Jährigen ist zu entnehmen, daß die Behörden diese Ergebnisse kleinzureden versuchen,
Nach der Zulassung des Pfizer-BioNTech COVID-19-Impfstoffs für Kinder im Alter von 5–11 Jahren im Oktober 2021 und der Verabreichung von etwa 8 Millionen Dosen wurden lokale und systemische Reaktionen nach der Impfung häufig an VAERS und v-safe für geimpfte Kinder im Alter von 5– 11 Jahre. Schwerwiegende unerwünschte Ereignisse wurden selten berichtet.
Eltern und Erziehungsberechtigte von Kindern im Alter von 5–11 Jahren sollten darauf hingewiesen werden, dass lokale und systemische Reaktionen nach der Impfung mit Pfizer-BioNTech COVID-19-Impfstoff zu erwarten sind und nach der zweiten Dosis häufiger auftreten.
Das folgende Video findet sich hier und hier.
Diese Position wiederholte er noch einmal auf FoxNews
.
Überprüfung der VAERS-Daten für 5-11-Jährige
Vom 3. November bis 19. Dezember 2021 erhielt und verarbeitete VAERS 4.249 Berichte über unerwünschte Ereignisse (Tabelle 1) für Kinder im Alter von 5 bis 11 Jahren, die den Pfizer-BioNTech COVID-19-Impfstoff erhielten; das Durchschnittsalter betrug 8 Jahre, und 1.896 (44,6 %) Meldungen betrafen Männer.
- Die meisten Kinder (4.143; 97,5 %) erhielten den Pfizer-BioNTech COVID-19-Impfstoff allein; Der saisonale Influenza-Impfstoff war der am häufigsten gleichzeitig verabreichte Impfstoff (91 [2,1 %] Kinder).
- Insgesamt betrafen 4.149 (97,6 %) VAERS-Meldungen nicht schwerwiegende Ereignisse und 100 (2,4 %) schwerwiegende Ereignisse.
„Nicht schwerwiegende Fälle“
- Das Durchschnittsalter der Kinder mit Berichten über nicht schwerwiegende Ereignisse betrug 8 Jahre, und 1.835 (44,2 %) dieser Berichte betrafen Männer.
- Die am häufigsten gemeldeten nicht schwerwiegenden Ereignisse standen im Zusammenhang mit der Impfstoffverabreichung (einige ohne unerwünschte Ereignisse), darunter keine unerwünschten Ereignisse (1.157; 27,9 %), Probleme bei der Produktzubereitung (925; 22,3 %) und falsche verabreichte Dosen (675; 16,3 %). , (Tabelle 2).
- Das Durchschnittsalter der Kinder mit Berichten über schwerwiegende Ereignisse betrug 9 Jahre, und 61 (61,0 %) der Berichte waren Männer.
„schwerwiegende Fälle“
- Die am häufigsten gemeldeten Erkrankungen und diagnostischen Befunde unter den 100 Meldungen über schwerwiegende Ereignisse waren Fieber (29; 29,0 %), Erbrechen (21; 21,0 %) und erhöhtes Troponin§§§ (15; 15,0 %).
- Unter den 12 schwerwiegenden Berichten über Krampfanfälle erlitt ein Kind eine Synkope (kein Krampfanfall) und ein weiteres Kind möglicherweise eine Synkope, zwei Kinder erlitten einen Fieberkrampf, ein Kind hatte Krampfanfälle in der Vorgeschichte, zwei Kinder hatten eine sich möglicherweise entwickelnde Anfallserkrankung und fünf Kinder erlebten neue -beginnende Anfälle.
- Von den 15 vorläufigen Berichten über Myokarditis, die während des Analysezeitraums identifiziert wurden, wurden 11 verifiziert (durch Befragung des Anbieters oder Durchsicht der Krankenakte) und erfüllten die Falldefinition für Myokarditis¶¶¶; Von diesen 11 Kindern erholten sich sieben und vier erholten sich zum Zeitpunkt des Berichts.
- VAERS erhielt während des Analysezeitraums zwei Todesberichte; beide werden überprüft. Diese Todesfälle traten bei zwei Frauen im Alter von 5 und 6 Jahren auf, die beide eine komplizierte Krankengeschichte hatten und sich vor der Impfung in einem schwachen Gesundheitszustand befanden.
Keine der Daten deutete auf einen kausalen Zusammenhang zwischen Tod und Impfung hin.
.
Je jünger die Impflinge, desto stärker die Nebenwirkungen
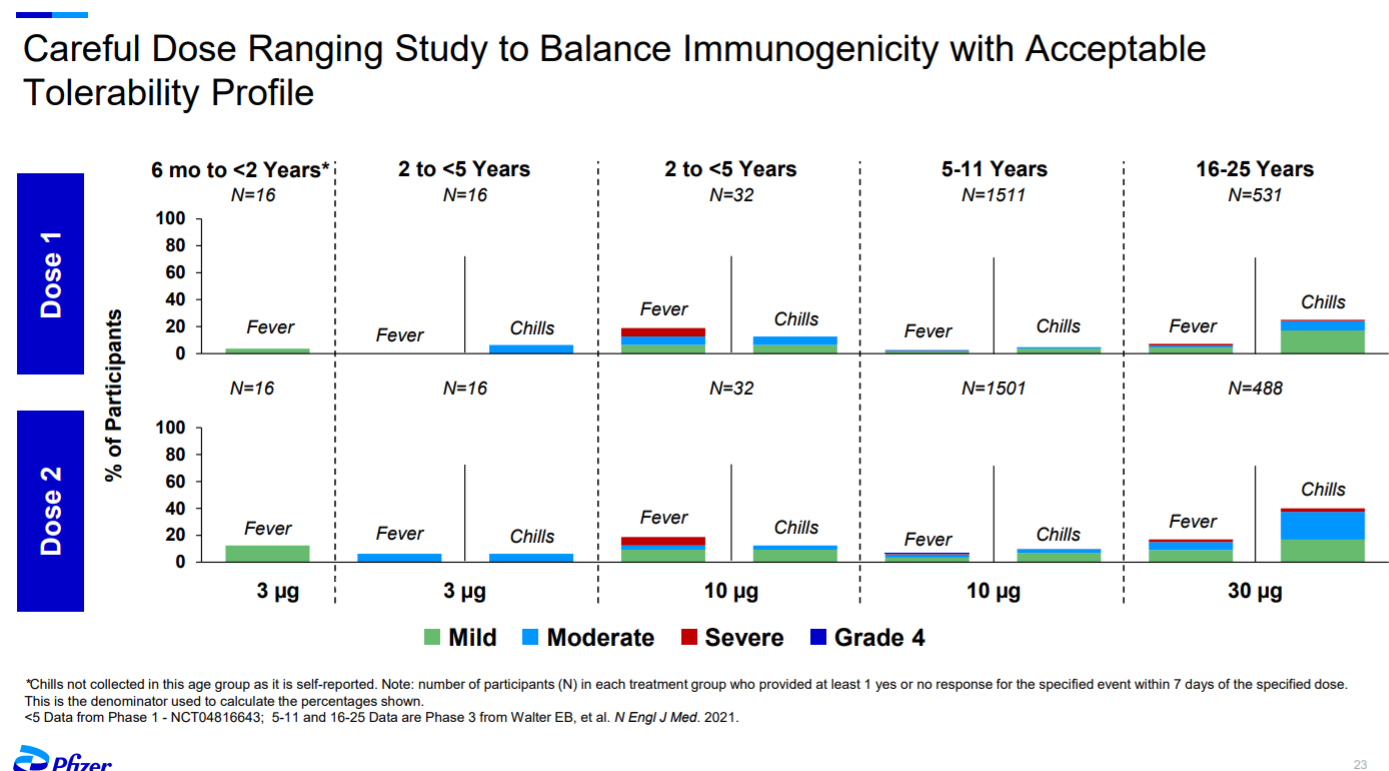
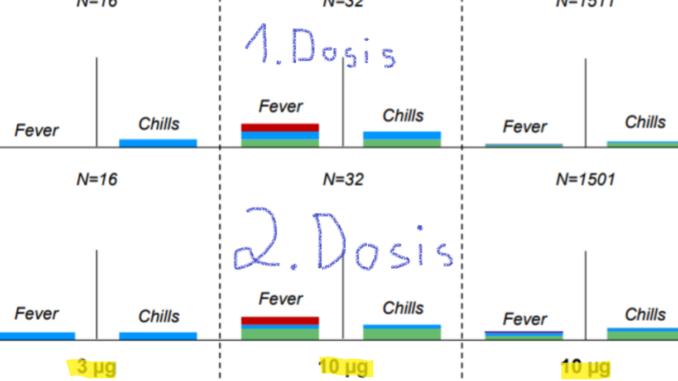
Einer Information für Investoren und Analysten kann man entnehmen, daß die Nebenwirkungen umso stärker werden, je jünger die Impflinge werden.
Der Abbildung rechts kann man entnehmen, daß die 5-11-Jährigen 10 Mikrogramm mRNA-Wirkstoff erhielten und die 2-5-Jährigen ebenso.
Der Abbildung ist auch zu entnehmen, daß bei den verabreichten 10 Mikrogramm mRNA viel öfter und viel schwereres Fieber auftrat, als bei älteren Kindern.
Diese Tatsache dürfte eine Rolle dabei gespielt haben, daß Pfizer bei den 2-5-Jährigen dann auf die 10 Mikrogramm-Dosis, die zweimal zu verabreichen wäre, verzichtete.
An Stelle 2* 10 Mikrogramm experimentierte man mit 2 Spritzen zu je 3 Mikrogramm mRNA-Wirkstoff, was der Menge entspricht, die ursprünglich für Kinder unter 2 Jahre vorgesehen war und dann für Kleinkinder bis 5 Jahre angewendet wurde.
Der Grund: Mit 3 Mikrogramm mRNA-Wirkstoff traten weniger Nebenwirkungen auf. Auf der anderen Seite ist fraglich, ob mit 3 Mikrogramm mRNA-Wirkstoff überhaupt irgend eine Wirkung zu erreichen.
.
Der Rückzug Pfizers von der Impfung der 0,5-2-Jährigen
Erst vor wenigen Tagen hatte Pfizer in den USA eine Zulassung für ihre mRNA-Wirkstoffe Unter-5-Jährige bei der US-amerikanischen Prüfungsbehörde FDA eingereicht gehabt. Der Konzern begehrte eine Notzulassung für Babys ab sechs Monaten. Nur eine Woche später zog der Pharmariese seinen Antrag zurück.
Pfizer will die internen Untersuchungen aber weiterühren, aber den Zulassungsantrag vorerst aussetzen nicht weiterführen. Laut Pfizer sei der Grund, daß man Kindern von 6 Monaten bis 5 Jahren nun drei Dosen verabreichen möchte, weswegen auch eine Zulassung verschoben werde.
Offenbar glaubt Pfizer selbst nicht daran, dieses Problem in absehbarer Zeit lösen zu können, denn sonst hätten sie ja die Zulassung nicht zurückgezogen.



Antworten